L-乳酸輸送体が基質を選択するメカニズムを解明~基質輸送経路に存在する2つの残基の重要な役割~
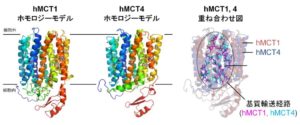 北海道大学大学院生命科学院博士課程・日本学術振興会特別研究員の二木悠哉氏,同大学大学院薬学研究院の井関 健教授らの研究グループは,ホモロジーモデリング法及び部位特異的変異導入法を用いて,ヒトモノカルボン酸輸送体1, 4(hMCT1, 4)の基質選択性に関わるアミノ酸残基を同定しました。
北海道大学大学院生命科学院博士課程・日本学術振興会特別研究員の二木悠哉氏,同大学大学院薬学研究院の井関 健教授らの研究グループは,ホモロジーモデリング法及び部位特異的変異導入法を用いて,ヒトモノカルボン酸輸送体1, 4(hMCT1, 4)の基質選択性に関わるアミノ酸残基を同定しました。
hMCT1, 4は,生体内でのエネルギー代謝に関わる化合物であるL-乳酸の輸送を担う輸送体です。これまでに,hMCT1はL-乳酸に加え5-オキソプロリンを輸送する一方で,hMCT4は5-オキソプロリンを輸送しないという知見が得られており,hMCT1とhMCT4の間にはその基質選択性の違いを決定する何らかの分子メカニズムの存在が予測されていました。そこで,研究グループはhMCT1, 4の予測3次元構造とアフリカツメガエル卵母細胞を用いたhMCT1, 4の輸送活性評価系を利用し,hMCT1選択的な5-オキソプロリン輸送に重要な2つのアミノ酸残基(69番目のメチオニン残基及び367番目のフェニルアラニン残基)を同定しました。
本研究により,hMCT1, 4の基質選択に関わるメカニズムの一端が明らかとなり,その構造と機能との関連に新たな知見を与えました。将来的に,L-乳酸輸送体が医薬品の新たな標的分子となることが期待されます。
なお,本研究成果は,2019年5月17日(金)にCellular and Molecular Life Sciences誌にオンライン掲載されました。
また,本研究は日本学術振興会科学研究費補助金(17J00013)の助成を受け,実施されました。
論文情報
論文名 Homology modeling and site-directed mutagenesis identify amino acid residues
underlying the substrate selection mechanism of human monocarboxylate transporters 1
(hMCT1)and 4(hMCT4)(ホモロジーモデリング法および部位特異的変異導入法を利用
したヒトモノカルボン酸輸送体 hMCT1, 4 の基質選択メカニズムに関与するアミノ酸残基の
同定)
著者名 二木悠哉 1,2,小林正紀 3,4,鳴海克哉 3,古堅彩子 3,井関 健 3,4(1北海道大学大学院生命
科学院, 2日本学術振興会特別研究員 DC, 3北海道大学大学院薬学研究院, 4北海道大学病
院薬剤部)
雑誌名 Cellular and Molecular Life Sciences(生物学,生物医学の専門誌)
DOI 10.1007/s00018-019-03151-z
公表日 2019 年 5 月 17 日(金)(オンライン公開)